Tumorschmerz
Tumorerkrankungen gehen oftmals mit Schmerzen einher. Diese werden meist mit Opioiden behandelt, welche jedoch nicht bei allen Patienten ausreichend effektiv sind.10
Die Effektivität von Cannabinoiden bei Tumorschmerz konnte bereits in einer randomisierten, kontrollierten Studie gezeigt werden: So konnte die Reduktion der Schmerzen auf den analgetischen Effekt der Cannabinoide zurückgeführt werden. Weitere Studien stützen diese Beobachtungen.10,11
Johnson et al. 2010
Multicenter, double-blind, randomized, placebo-controlled, parallel-group study of the efficacy, safety, and tolerability of THC:CBD extract and THC extract in patients with intractable cancer-related pain10
Die Studie verglich die Wirksamkeit eines THC:CBD-Extrakts mit einem THC-Extrakt und Placebo bei Patienten mit Tumorschmerzen, ausgelöst durch einen Tumor im fortgeschrittenen Stadium, deren Schmerzen trotz chronischer Opioidtherapie unzureichend gelindert wurden.
| Art der Studie: | RCT (multizentrisch, doppelblind, Placebo-kontrolliert) |
| Studiendesign: |
|
| Studiendauer: | 2 Wochen + 2 Tage Baseline |
| Studienendpunkte: | Co-primäre Endpunkte:
|
Ergebnisse
- Signifikante Verbesserung der Numerical Rating Scale (NRS) unter THC:CBD gegenüber Placebo (-1,37 vs. -0,69; Δ 0,67)
- NRS-Schmerzreduktion um > 30 % unter THC:CBD bei doppelt so vielen Patienten wie unter Placebo (43 % vs. 21 %)
Ansprechraten entsprechend Verbesserung auf einer numerischen Schmerzskala (0-10)
- Keine signifikante Veränderung der Schmerzintensität unter THC vs. Placebo
- Keine signifikanten Unterschiede in der Schlafqualität, Übelkeit oder Schmerzkontrolle nach NRS zwischen den Gruppen. Schlaf verbesserte sich in allen Gruppen leicht, numerisch etwas stärker unter Sativex®
- Signifikanter Anstieg der Durchbruchmedikation in der Placebogruppe ggü. THC:CBD (7 vs. 2 Patienten, p = 0,004), Opioid-Hintergrundmedikation veränderte sich nicht
- THC:CBD-Extrakt ist effektiv zur Schmerzreduktion bei Patienten mit Tumorschmerzen, die durch starke Opioide nicht kontrollierbar sind
Verträglichkeit
- Nebenwirkungen waren meist mild oder moderat
Portenoy et al. 2012
Nabiximols for Opioid-Treated Cancer Patients With Poorly-Controlled Chronic Pain: A Randomized, Placebo-Controlled, Graded-Dose Trial12
Die Studie untersuchte die Wirkung eines THC:CBD-Extrakts (Nabiximols) bei Patienten mit fortgeschrittener Krebserkrankung, deren Tumorschmerzen durch Opioide nicht ausreichend kontrolliert werden konnten.
Studiendesign
| Art der Studie: | RCT (doppelblind, Placebo-kontrolliert, Dosierung gestaffelt) |
| Studiendesign: |
|
| Studiendauer: | 9 Wochen:
|
| Studienendpunkte: |
Primärer Wirksamkeitsendpunkt:
Sekundäre Endpunkte:
|
Ergebnisse
- Primäre Analyse (Anteil der Patienten mit 30 % Schmerzreduktion) ergab keinen signifikanten Unterschied zwischen Nabiximols und Placebo
- Sekundäre Responder-Analyse: größerer Anteil der Patienten mit Schmerzreduktion unter Nabiximols als unter Placebo (p = 0,035)
Analyse der Veränderung zur Baseline auf einer numerischen Schmerzskala (0–10).
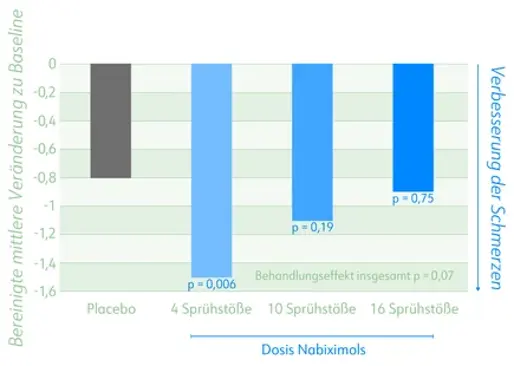
-
Signifikante Verbesserung der Schlafqualität über alle Behandlungsgruppen (p = 0,003), am stärksten ausgeprägt in der niedrigsten Dosierung
Verträglichkeit
- Nebenwirkungen waren dosisabhängig: Gruppe mit der hohen Dosis schnitt im Vergleich mit Placebo schlechter ab (Patienten mit Nebenwirkungen: niedrige Dosis 77 %, mittlere Dosis 85 %, hohe Dosis 92 % vs. 78 % bei Placebo)
Fazit
Studie demonstrierte Sicherheit und Wirksamkeit von niedrigen/moderaten Cannabinoid-Dosen in der Add-on-Therapie von Tumorschmerzen



